
|
|
|||||
|
||||||
藥改20年,從大降價到進口替代摘要:
醫藥網4月10日訊 在大部制開啟、醫療衛生和醫藥產業主管部門重大調整之際,回顧20多年來藥品經歷的主要改革,大致可分為四個階段。
階段一 (1996年始)
▍藥品降價:難解“看病貴”
行政降價(1996-2015.5)
從1996年國家計委出臺《藥品價格管理暫行辦法》,到2015年發改委等七部委發布《關于印發推進藥品價格改革意見的通知》要求自2015年6月1日起放開政府定價,這20年間共進行了32次藥品行政性降價(見圖1),累計降價近千億元。
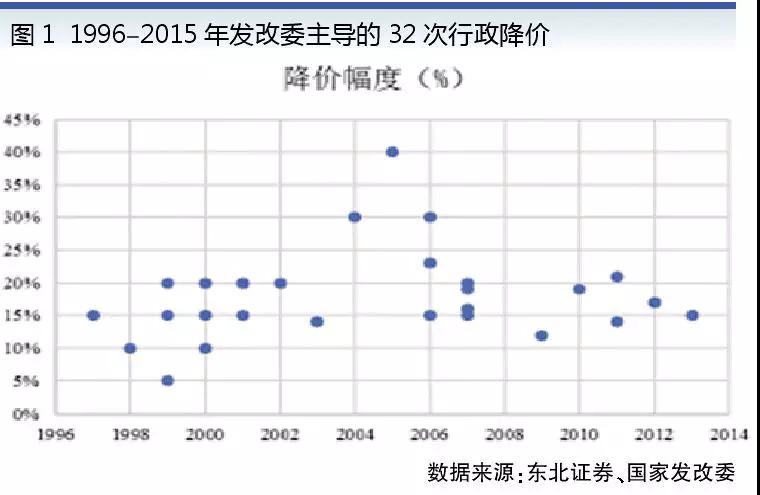 2001年,衛生部等六部委發布《醫療機構藥品集中招標采購工作規范(試行)》,使藥品集中招標采購工作在全國全面推行。作為無奈之舉的藥品招標,越來越變成以降價為唯一目標,而一旦按病種付費政策落地,招標將不再有意義。醫療保障局的成立,更會對其進行調整,但目前招標仍是常態。
招標導致藥品降價幅度逐年加劇,僅以2015-2017年為例,招標降價的幅度就依次增加到23.4%、28.5%和36.6%(見圖2)。
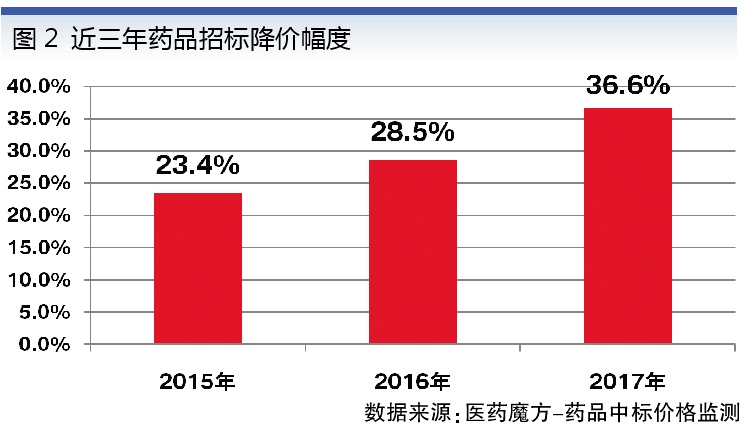 二十多年來的多次行政降價、藥品招標并沒有解決看病貴的問題,反而很多常用藥變成了短缺藥。
階段二 (2009年始)
▍基藥制度:用藥限制漸被打破
國家發改委、衛生部等九部委于2009年8月18日發布的《關于建立國家基本藥物制度的實施意見》,標志著我國建立國家基本藥物制度工作的正式實施。
兩次黨代會和中辦國辦文件也強調了基本藥物制度的重要性(見表1),并且規定,基本藥物全部納入基本藥品保障報銷目錄,報銷比例明顯高于非基本藥物,還對各級醫療機構規定了最低使用比例。其間,政府還投入了8500億元以健全基本醫療衛生服務體系,建立基本藥物制度等,基藥銷量也逐年大幅提升(見圖3)。
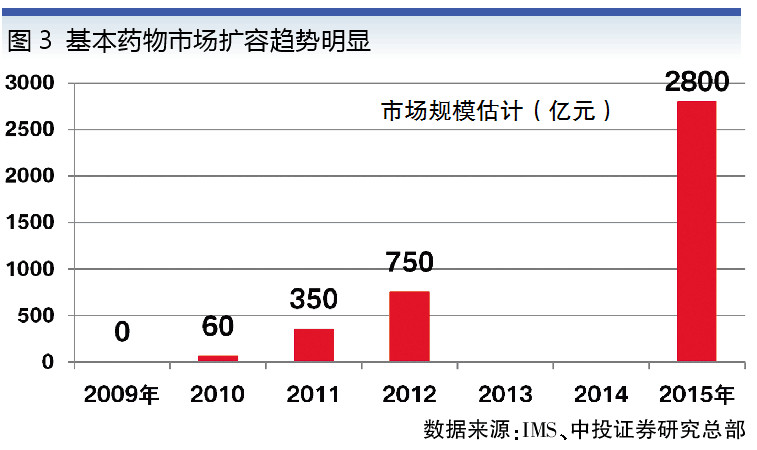 如今,隨著分級診療制度的推進,出于承接大醫院轉診患者的需要,基層醫療機構用藥的限制也逐漸被打破。
階段三 (2015年始)
▍鼓勵創新:審評審批大提速
2015年8月,國務院出臺《關于改革藥品醫療器械審評審批制度的意見》(國發 2015 44號)標志著以鼓勵創新為主的藥品醫療器械審評審批制度改革正式開始。
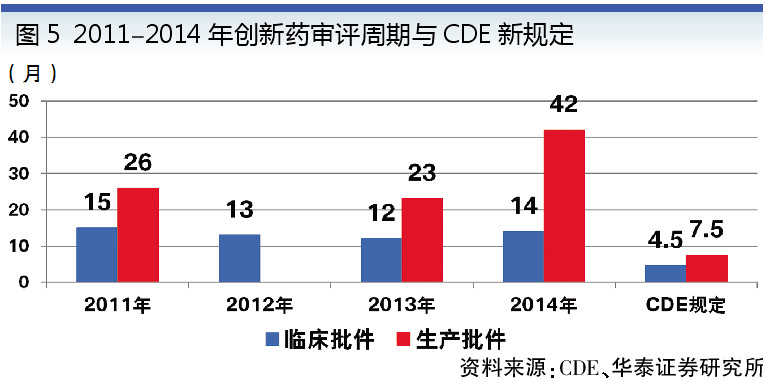
此次改革效果顯著:提高了審評質量和標準,整治了科研造假不良風氣,提高了審評審批透明度,藥品審評積壓問題如期解決(見圖4),新藥審評周期大幅縮短(見圖5),仿制藥質量和療效一致性評價順利起步。
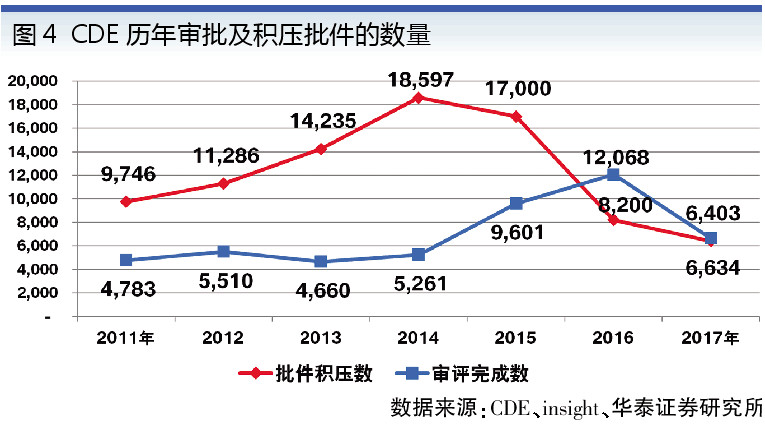  階段四 (2017年始)
▍原研替代:未來控費利器
隨著老齡化加劇、醫保覆蓋人群進一步加大,醫保資金越發緊張,控費成為今后的重要任務。近年相繼出臺的降低藥占比、輔助用藥目錄、重點監控目錄等無不圍繞控費展開,盡管也已取得了一定的效果,但并非治本之策。
按病種付費被多國證明是有效的控制藥費的好方法,而DRGs(Diagnosis Related Groups,即疾病診斷相關分類)作為按病種付費的分支,是當今世界公認的比較先進的支付方式之一。
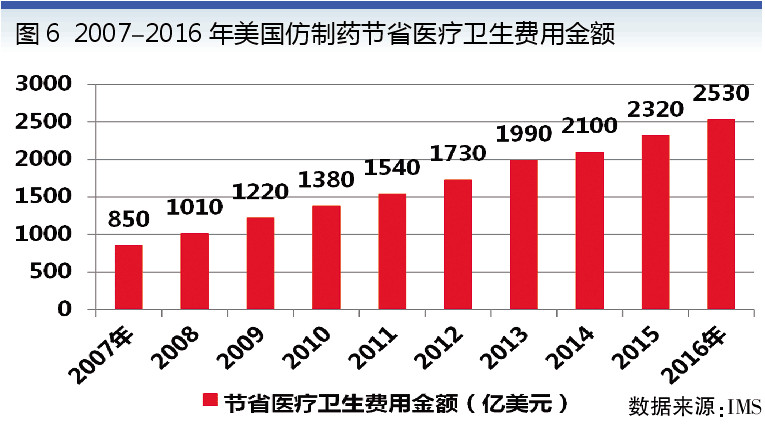
美國實施DRGs后,人均醫療費用支出增速得到了明顯控制。其核心在于使醫院有動力在確保療效與原研藥相同的前提下,大量使用價格更低的仿制藥來替代原研藥。十年時間,美國仿制藥替代原研為國家節省了1.67萬億美元的醫療支出(見圖6)。
 DRGs的實施必將刺激仿制藥的加速發展,而發展仿制藥有兩條主要途徑:一是對16萬多個存量批文進行仿制藥一致性評價,二是加速對原研藥的仿制,相應地需要建立上市藥品目錄集、專利鏈接、專利期限補償、數據保護等制度。
這在去年發布的《關于深化審評審批制度改革鼓勵藥品醫療器械創新的意見》已有提及,國務院辦公廳于今年4月3日發布的《關于改革完善仿制藥供應保障及使用政策的意見》(國辦發〔2018〕20號)在促進仿制藥研發、提升仿制藥質量療效等方面也提出了詳細措施。
筆者相信,DRGs激勵醫院主動進行原研替代,加之新成立的醫療保障局實現三保合一綜合統籌,“看病貴”頑疾這次真能根治。
|
|
Copyright ?2015 廣東穗康醫藥有限公司
粵ICP備15022662號(粵)
-技術支持:信息管理部|聯系我們
|